Ácido fórmico: estructura y propiedades químicas
Con respecto a la pregunta sobre ¿dónde encontrar ácido fórmico?, hay que decir que la respuesta está en las hormigas. Puesto que durante más de 600 años los naturalistas supieron que los hormigueros emitían un vapor ácido. En 1671, el naturalista inglés John Ray describió el aislamiento del ingrediente activo.
Para ello recogió y destiló un gran número de hormigas muertas, y el ácido que descubrió más tarde se conoció como ácido fórmico de la palabra latina para hormiga, formica.
La primera síntesis de este ácido fue realizada por el químico francés Joseph Gay-Lussac, que usó ácido cianhídrico como material de partida. En 1855, otro químico francés, Marcellin Berthelot, desarrolló una síntesis a partir del monóxido de carbono que es similar a la que se utiliza hoy en día.
El ácido fórmico también está presente en estado natural en las ortigas que pican, y es responsable de la sensación de ardor al contacto con ellas. También se encuentra en las picaduras y mordeduras de muchos insectos, incluidas abejas y hormigas, que lo utilizan como mecanismo de defensa química.
Cuando la hormiga contrae su glándula del veneno, el ácido almacenado en esta glándula pasa por el aguijón y es propulsado en chorros (hasta una distancia de un metro en algunas especies) hacia los atacantes de la hormiga.
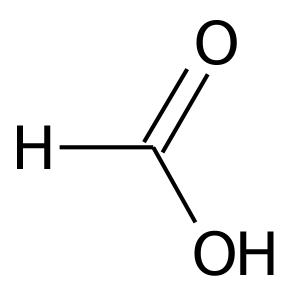
Estructura del ácido fórmico
La fórmula química del ácido fórmico es HCOOH, y es una molécula plana. El ácido fórmico es un líquido incoloro y humeante que es miscible con agua. En la fase de vapor, está formado por dímeros enlazados con hidrógeno (ver foto, derecha) en lugar de moléculas individuales.
En la fase gaseosa, surgen importantes desviaciones de la ley del gas ideal como resultado de este enlace de hidrógeno. En su estado líquido y sólido, el ácido fórmico puede considerarse como una red efectivamente infinita de moléculas enlazadas con hidrógeno.
Propiedades químicas
Siendo el primero de la serie de ácidos carboxílicos, el ácido fórmico comparte la mayoría de las mismas propiedades químicas, y por lo tanto reaccionará con los álcalis para formar sales de formiato solubles en agua. Pero el ácido fórmico es único entre los ácidos carboxílicos porque reacciona con los alquenos para formar ésteres de formiato.
En presencia de los ácidos sulfúricos e hidrofluóricos, una variante de la reacción de Gatterman-Koch tiene lugar en vez de la común, y el ácido fórmico se añade al alqueno para producir un ácido carboxílico más grande.